L’amilosio è un polisaccaride formato da unità di α-D-glucosio legate da legami glicosidici α-(1→4), con poche ramificazioni connesse alla catena principale da legami glicosidici α-(1→6).[17]
Insieme all’amilopectina è uno dei due principali costituenti dell’amido, la più diffusa e abbondante forma di accumulo di energia e carboidrati presente nella Biosfera.[12]
La sua sintesi è catalizzata dall’enzima amido sintasi legata ai granuli o GBSS (EC 2.4.1.242), e necessita della presenza di una seconda proteina, la PTST1, che è priva di attività catalitica.[15]
Nel granulo di amido l’amilosio viene depositato all’interno della matrice semicristallina formata dall’amilopectina.[13] Sebbene a differenza dell’amilopectina l’amilosio non sia necessario per la formazione dei granuli semicristallini di amido, dove è presente in quantità inferiore rispetto all’amilopectina, l’amilosio ha una grande influenza sulle proprietà fisico-chimiche dell’amido.[7]
Sono state selezionate piante dove il granulo di amido può contenere quantità molto piccole di amilosio, e altre dove invece i granuli sono formati per la quasi totalità dal polisaccaride. Questi fenotipi possono avere vantaggi sia dal punto di vista della salute che industriale.[4][20]
Indice
- Struttura
- Localizzazione dell’amilosio nel granulo di amido
- Sintesi
- Rapporto amilosio-amilopectina
- Amidi ricchi di amilosio
- Bibliografia
Struttura
Le molecole di amilosio hanno un peso molecolare di circa 106 daltons, sono per la maggior parte lineari e formate da residui di α-D-glucosio, di seguito indicato come glucosio, legati a mezzo di legami glicosidici α-(1→4), ossia legami in cui ciascuna unità glucosidica è legata alla successiva a mezzo di un legame covalente tra il C-1 di una unità e il gruppo ossidrilico sul C-4 dell’unità successiva.[1] Le catene lineari sono costituite da un numero di monosaccaridi variabile da poche centinaia a diverse migliaia, risultando quindi molto più lunghe di quelle dell’amilopectina.[17]
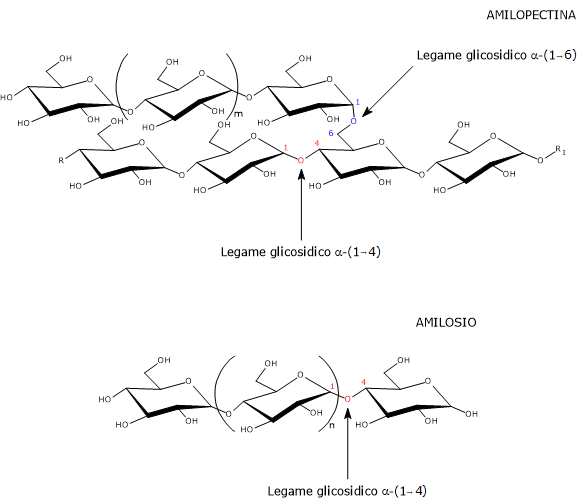 Le poche ramificazioni sono connesse alla catena lineare da legami glicosidici α-(1→6), al pari di quanto accade con l’amilopectina e il glicogeno, la forma di accumulo dei carboidrati presente negli animali. Nel caso dei legami glicosidici α-(1→6), le due unità di glucosio sono unite da un legame covalente tra il C-1 di un’unità e il gruppo ossidrilico sul C-6 dell’altra unità. Il numero di ramificazioni è compreso tra 5 e 20, a seconda dell’origine botanica dell’amido, ramificazioni che, rispetto all’amilopectina, non sono raggruppate.[6] Studi sulla lunghezza delle ramificazioni dell’amilosio hanno evidenziato una loro distribuzione bimodale, con le due frazioni indicate come:
Le poche ramificazioni sono connesse alla catena lineare da legami glicosidici α-(1→6), al pari di quanto accade con l’amilopectina e il glicogeno, la forma di accumulo dei carboidrati presente negli animali. Nel caso dei legami glicosidici α-(1→6), le due unità di glucosio sono unite da un legame covalente tra il C-1 di un’unità e il gruppo ossidrilico sul C-6 dell’altra unità. Il numero di ramificazioni è compreso tra 5 e 20, a seconda dell’origine botanica dell’amido, ramificazioni che, rispetto all’amilopectina, non sono raggruppate.[6] Studi sulla lunghezza delle ramificazioni dell’amilosio hanno evidenziato una loro distribuzione bimodale, con le due frazioni indicate come:
- AM1, che raggruppa le catene più corte, con un grado di polimerizzazione compreso tra i 100 e i 700 daltons;
- AM2, dove si ritrovano le catene più lunghe, con un grado di polimerizzazione compreso tra i 700 e i 40.000 daltons.[19]
Analoga distribuzione bimodale della lunghezza delle ramificazioni si osserva nell’amilopectina, le cui frazioni sono indicate come AP1, più corte e abbondanti, e AP2.
La variazione intraspecie della distribuzione delle frazioni AM1 e AM2 è relativamente piccola, mentre è grande tra specie differenti, variazioni che hanno una base genetica.[19]
Localizzazione dell’amilosio nel granulo di amido
L’esatta localizzazione dell’amilosio all’interno del granulo di amido non è nota, sebbene si ritenga che la maggior parte si trovi nelle regioni amorfe. Tuttavia alcuni studi hanno suggerito che la sua localizzazione non sia limitata alle regioni amorfe, ma sia anche presente tra le catene di amilopectina e sulla superficie dei granuli.[13] Ne consegue che l’amilosio potrebbe avere diverse localizzazione all’interno del granulo di amido.
Sintesi
Nelle piante la sintesi dell’amilosio è catalizzata dalla GBSS, una selle sei isoforme dell’amido sintasi.[11] L’enzima, la cui azione è la principale determinante del contenuto in amilosio del granulo di amido, necessita della presenza della proteina PTST1.[15] L’inserzione delle ramificazioni sembra essere catalizzata dall’enzima ramificante l’amido o SBE (EC 2.4.1.18).
Come nel caso della sintesi dell’amilopectina, si ritiene che gli enzimi coinvolti interagiscano fisicamente a formare complessi multienzimatici, strutture in grado di ottimizzare l’efficienza dell’intero processo.[17]
Poiché la sintesi dell’amilosio necessita della presenza di un’impalcatura di amilopectina per poter indirizzare l’amido sintasi legata ai granuli verso i granuli di amido, la sintesi dei due polisaccaridi non è del tutto contemporanea.[11]
Nelle fasi iniziali, l’amido sintasi legata ai granuli, al pari delle altre amido sintasi, necessita della presenza di corti malto-oligosaccaridi o MOS, α-(1→4)-glucani lunghi da 2 a 7 residui glucosidici, che fungono da primer e sono allungati.[17] I MOS possono originare da diverse fonti, tra cui il processo di rifinitura di molecole di amilopectina nascenti per opera dell’enzima deramificante, o dall’attività dell’amido fosforilasi (EC 2.4.1.1), un altro enzima coinvolto nel metabolismo dell’amido.[16] Essendo scarsamente solubili in acqua, i MOS sembrano in grado di eludere l’azione idrolitica delle alfa-amilasi (EC 3.2.1.1) e delle beta-amilasi (EC 3.2.1.2), e diffondono all’interno della matrice dei granuli di amido in formazione dove sono allungati per azione della GBSS.[14] Una volta superati i sette residui glucosidici non riescono a diffondere facilmente al di fuori del granulo e sono ulteriormente allungati.
La fase iniziale della sintesi dell’amilosio e dell’amilopectina, richiedendo la presenza di un primer, somiglia a quella del glicogeno. Tuttavia, il primer richiesto nel corso della sintesi del glicogeno non è un oligosaccaride ma una proteina auto-glicosilante, la glicogenina.
Da notare che la polimerizzazione del glucosio in amilopectina, amilosio, o glicogeno, e più in generale di monosaccaridi osmoticamente attivi in polisaccaridi osmoticamente inerti, permette il deposito di grandi quantità di molecole osmoticamente attive all’interno della cellula senza che si verifichi un aumento della pressione osmotica.
Amido sintasi legata ai granuli
GBSS e le altre isoforme dell’amido sintasi appartengono alla famiglia delle glicosiltransferasi (EC 2.4), al pari dell’amido fosforilasi.[11]
L’enzima, scoperto dal gruppo di Louis Federico Leloir, che in precedenza aveva scoperto la principale via per il metabolismo del galattosio, la via di Leloir, è la più abbondante tra le proteine associate ai granuli di amido.[9] E’ presente quasi esclusivamente legata ai granuli, a differenza delle altre isoforme della amido sintasi che sono per la maggior parte presenti nello stroma del plastidio, o suddivise tra stroma e granuli. Inoltre, il trattamento della superficie dei granuli con proteasi ha evidenziato che la maggior parte di GBSS è presente all’interno del granulo piuttosto che sulla sua superficie, posizionamento coerente con la sintesi dell’amilosio all’interno dei granuli nascenti.[15]
Nelle graminacee la sintasi è presente in due isoforme, codificate da geni distinti, indicate come GBSSI e GBSSII, presenti rispettivamente negli amiloplasti dei tessuti di deposito, quindi non fotosintetici, e nei cloroplasti, quindi nei tessuti fotosintetici dove interviene nella sintesi dell’amido transiente.[18]
GBSS catalizza il trasferimento di una molecola di glucosio dall’ADP-glucosio all’estremità non riducente di un α-(1→4)-glucano, cui l’unità glucosidica viene legata attraverso un legame glicosidico α-(1→4).[5]
[(1→4)-alfa-D-glucosile](n) + ADP-alfa-D-glucosio ⇌ [(1→4)-alfa-D-glucosile](n+1) + ADP + H(+)
Si noti che, mentre le amido sintasi utilizzano come donatore dell’unità glucosidica l’ADP-glucosio, la glicogeno sintasi, che interviene nella sintesi del glicogeno, utilizza l’UDP-glucosio.[3]
L’amido sintasi legata ai granuli è in grado di aggiungere più di un’unità di glucosio per incontro con il substrato, modalità d’azione definita processiva, a differenza delle altre isoforme di amido sintasi che aggiungono una sola unità di glucosio per incontro con la catena di glucano nascente, azione definita distributiva. L’azione processiva permette la sintesi di lunghe catene lineari, e sembra essere fortemente incrementata dalla presenza di amilopectina.[17]
PTST1
La sintesi dell’amilosio richiede la presenza di una proteina della famiglia PTST, ossia PTST1, scoperta cinquanta anni dopo GBSS.[15]
PTST1 non ha attività catalitica, ma permette il legame di GBSS al granulo di amido, azione che sembra essere più importante nei cloroplasti, e quindi per la sintesi dell’amido transiente, che negli amiloplasti. Secondo un modello di azione di PTST1, la proteina si associa a GBSS nello stroma del plastidio, il complesso si lega al granulo di amido nascente, PTST1 si dissocia dall’enzima che inizia la sintesi dell’amilosio, mentre la proteina torna nello stroma per reclutare un’altra molecola di enzima.
L’importanza di PTST1 è sottolineata dal fatto che è conservata in tutto il regno vegetale e la sua perdita causa il distacco dell’enzima dal granulo di amido nascente.
Enzima ramificante l’amido
Non è noto l’enzima che catalizza l’inserzione delle poche ramificazioni presenti nelle molecole di amilosio, sebbene sembra possa essere coinvolta un’isoforma dell’enzima ramificante l’amido, la SBEI.[13]
Presente per la maggior parte nello stroma dei plastidi, e in piccola parte legato al granulo, è principalmente espressa nei tessuti di deposito. La bassa frequenza con cui sono presenti le ramificazioni nell’amilosio potrebbe essere il risultato della sintesi del polisaccaride all’interno dei granuli, dove la molecola nascente sarebbe protetta dall’azione dell’enzima ramificante l’amido, ivi scarsamente presente.[8]
Rapporto amilosio/amilopectina
Nei granuli di amido delle piante terrestri l’amilosio è quasi sempre presente, ma in percentuali variabili, in genere comprese tra il 5 e il 35%.[5] La variabilità si osserva non solo tra specie differenti, ma anche all’interno di una stessa specie in base all’organo o tessuto considerato, e, nei tuberi e semi, in base alla fase di sviluppo, essendo in genere il suo contenuto basso nelle prime fasi, per poi aumentare fino al raggiungimento del valore finale, una modalità coerente con la sua sintesi all’interno di una matrice di amilopectina.[13]
Esistono tuttavia piante il cui contenuto di amilosio è molto basso, o addirittura assente. I loro amidi sono detti cerosi, per l’aspetto simile a cera dell’endosperma dei chicchi crudi. Al contrario, ci sono piante i cui granuli di amido sono formati per la maggior parte, o in alcuni casi per la quasi totalità, da amilosio.[20]
Sebbene il suo ruolo biologico non sia ancora stato chiarito, la sua quasi costante presenza sembra indicare che questo polisaccaride svolga un ruolo strutturale importante nel granulo di amido, e conferisca alla pianta un qualche vantaggio nella fase di crescita e sviluppo.[13]
Il rapporto amilosio/amilopectina influenza fortemente le proprietà fisico-chimiche dell’amido, quali la sua capacità di assorbire acqua, che a sua volta influenza processi come la gelatinizzazione e la retrogradazione dell’amido, o la resistenza all’idrolisi enzimatica, quest’ultima importante ad esempio nel determinare la velocità con cui il maltosio e maltotriosio sono rilasciati per azione della alfa-amilasi e delle beta-amilasi.[10] Tutto ciò è in grado di influenzare gli utilizzi industriali dell’amido nonché i suoi effetti sulla salute.
Amidi ricchi di amilosio
I cerali ad alto contenuto di amilosio sono ottenuti attraverso l’aumento dell’espressione del gene per GBSSI, e dalla soppressione o eliminazione dei geni codificanti l’enzima ramificante l’amido, SSIIa, o altri enzimi e proteine coinvolti nella sintesi dell’amilopectina. Tuttavia, almeno per l’endosperma dei cereali, la metodica più efficace è risultata essere la soppressione o l’eliminazione di una o più isoforme dell’enzima ramificante l’amido.[4][20]
Gli amidi ad alto contenuto di amilosio hanno proprietà chimico-fisiche peculiari, tra cui una elevata forza gelificante, una maggior facilità di retrogradazione, e un’ottima capacità di formare film, caratteristiche che li rendono idonei ad applicazioni industriali come la produzione di plastica biodegradabile, di carta e di adesivi.[7][10]
Gli amidi ricchi in amilosio sono ricchi di amido resistente, un tipo di amido che resiste alla digestione intestinale ad opera della alfa-amilasi, una delle idrolasi coinvolte nella digestione dei carboidrati. Studi condotti utilizzando cibi arricchiti con amido resistente hanno evidenziato un miglioramento delle risposte insuliniche e glicemiche, nonché una riduzione del rischio di sviluppare malattie cardiovascolari, obesità e diabete mellito di tipo II.[2]
Quale potrebbe essere la loro modalità d’azione?
L’amido resistente, essendo in grado di eludere l’azione dell’alfa-amilasi, potrebbe ridurre l’indice glicemico degli alimenti in cui è presente, contribuendo così a una migliore regolazione della glicemia. Inoltre, una volta raggiunto il colon, l’amido resistente può essere fermentato dai batteri del microbiota intestinale, che è parte del più ampio microbiota umano, con produzione di acidi grassi a catena corta, in particolari l’acido butirrico, l’acido acetico e l’acido propionico, acidi grassi essenziali per la salute intestinale.
Bibliografia
- ^ Bertoft E. Understanding starch structure: recent progress. Agronomy 2017;7:56. doi:10.3390/agronomy7030056
- ^ Birt D.F., Boylston T., Hendrich S., Jane J.L., Hollis J., Li L., McClelland J., Moore S., Phillips G.J., Rowling M., Schalinske K., Scott M.P., Whitley E.M. Resistant starch: promise for improving human health. Adv Nutr 2013;4(6):587-601. doi:10.3945/an.113.004325
- ^ Crofts N., Abe N., Oitome N.F., Matsushima R., Hayashi M., Tetlow I.J., Emes M.J., Nakamura Y., Fujita N. Amylopectin biosynthetic enzymes from developing rice seed form enzymatically active protein complexes. J Exp Bot 2015;66(15):4469-82. doi:10.1093/jxb/erv212
- ^ a b Funnell-Harris D.L., Sattler S.E., O’Neill P.M., Eskridge K.M., and Pedersen J.F. Effect of waxy (low amylose) on fungal infection of Sorghum grain. Phytopathology 2015;105(6):716-846. doi:10.1094/PHYTO-09-14-0255-R
- ^ a b Gous P.W., Fox G.P. Review: amylopectin synthesis and hydrolysis – Understanding isoamylase and limit dextrinase and their impact on starch structure on barley (Hordeum vulgare) quality. Trends Food Sci Technol 2016;62:23-32. doi:10.1016/j.tifs.2016.11.013
- ^ Hizukuri S., Takeda Y., Yasuda M., Suzuki A. Multi-branched nature of amylose and the action of debranching enzymes. Carbohydr Res 1981;94:205-213. doi:10.1016/S0008-6215(00)80718-1
- ^ a b Jobling S. Improving starch for food and industrial applications. Curr Opin Plant Biol 2004;7(2):210-8. doi:10.1016/j.pbi.2003.12.001
- ^ Kram A.M., Oostergetel G.T., Van Bruggen E. Localization of branching enzyme in potato tuber cells with the use of immunoelectron microscopy. Plant Physiol 1993;101(1):237-243. doi:10.1104/pp.101.1.237
- ^ Leloir L.F., de Fekete M.A., Cardini C.E. Starch and oligosaccharide synthesis from uridine diphosphate glucose. J Biol Chem 1961;236:636-41. doi:10.1016/S0021-9258(18)64280-29
- ^ a b Magallanes-Cruz P.A., Flores-Silva P.C., Bello-Perez L.A. Starch structure influences its digestibility: a review. J Food Sci 2017;82(9):2016-2023. doi:10.1111/1750-3841.13809
- ^ a b c Pfister B., Zeeman S.C. Formation of starch in plant cells. Cell Mol Life Sci 2016;73(14):2781-807. doi:10.1007/s00018-016-2250-x
- ^ Qu J., Xu S., Zhang Z., Chen G., Zhong Y., Liu L., Zhang R., Xue J., Guo D. Evolutionary, structural and expression analysis of core genes involved in starch synthesis. Sci Rep 2018;8(1):12736. doi:10.1038/s41598-018-30411-y
- ^ a b c d e Seung D. Amylose in starch: towards an understanding of biosynthesis, structure and function. New Phytol 2020;228:1490-1504. doi:10.1111/nph.16858
- ^ Seung D., Boudet J., Monroe J., Schreier T.B., David L.C., Abt M., Lu K.J., Zanella M., Zeeman S.C. Homologs of PROTEIN TARGETING TO STARCH control starch granule initiation in Arabidopsis leaves. Plant Cell 2017;29(7):1657-1677. doi:10.1105/tpc.17.00222
- ^ a b c d Seung D., Soyk S., Coiro M., Maier B.A., Eicke S., Zeeman S.C. PROTEIN TARGETING TO STARCH is required for localising GRANULE-BOUND STARCH SYNTHASE to starch granules and for normal amylose synthesis in Arabidopsis. PLOS Biol 2015;13(2):e1002080. doi:10.1371/journal.pbio.1002080
- ^ Szydlowski N., Ragel P., Raynaud S., Lucas M.M., Roldán I., Montero M., Muñoz F.J., Ovecka M., Bahaji A., Planchot V., Pozueta-Romero J., D’Hulst C., Mérida A. Starch granule initiation in Arabidopsis requires the presence of either class IV or class III starch synthases. Plant Cell 2009;21(8):2443-57. doi:10.1105/tpc.109.066522
- ^ a b c d e Tetlow I.J., Bertoft E. A review of starch biosynthesis in relation to the building block-backbone model. Int J Mol Sci 2020;21(19):7011. doi:10.3390/ijms21197011
- ^ Vrinten P.L., Nakamura T. Wheat granule-bound starch synthase I and II are encoded by separate genes that are expressed in different tissues. Plant Physiol 2000;122(1):255-64. doi:10.1104/pp.122.1.255
- ^ a b Wang K., Hasjim J., Wu A.C., Henry R.J., Gilbert R.G. Variation in amylose fine structure of starches from different botanical sources. J Agric Food Chem 2014;62(19):4443-53. doi:10.1021/jf5011676
- ^ a b c Wang J., Hu P., Chen Z., Liu Q., Wei C. Progress in high-amylose cereal crops through inactivation of starch branching enzymes. Front Plant Sci 2017;8:469. doi:10.3389/fpls.2017.00469