L’olio di oliva è un grasso alimentare ottenuto dalla spremitura delle olive, i frutti dell’albero di ulivo (Olea europaea).[1][2]
È un elemento fondamentale della dieta mediterranea ed è ampiamente utilizzato per cucinare, condire insalate e per altri scopi culinari. L’olio d’oliva è anche noto per i suoi benefici per la salute, poiché è ricco di grassi monoinsaturi e antiossidanti.[3]
Dal punto di vista chimico, nell’olio di oliva è possibile individuare, sulla base del comportamento in presenza di soluzioni fortemente alcaline e calore, due frazioni:
- la frazione saponificabile, che rappresenta il 98−99% del peso totale ed è formata da lipidi che, nelle condizioni suddette, formano saponi;
- la frazione insaponificabile, che costituisce il restante 1−2% del peso totale e che, nelle condizioni suddette, non forma saponi.[4][5]
Indice
Frazione saponificabile
È composta da acidi grassi saturi e acidi grassi insaturi, quasi per intero esterificati al glicerolo a formare trigliceridi o triacilgliceroli. In misura molto minore si ritrovano anche digliceridi (o diacilgliceroli), monogliceridi (o monoacilgliceroli), e acidi grassi liberi.[4]
Gli acidi grassi insaturi costituiscono il 75−85% del totale degli acidi grassi, mentre gli acidi grassi saturi il restante 15−25%.
I più abbondanti sono l’acido oleico (O) e l’acido linoleico (L); l’acido palmitoleico, l’acido eptadecenoico, l’acido gadoleico e l’acido alfa-linolenico (Ln) sono presenti in quantità inferiori o in tracce.[6]
| Acido grasso | Numero di carboni | Intervallo consentito (%) |
|---|---|---|
| Acido miristico | C14:0 | <0,03 |
| Acido palmitico | C16:0 | 7,5−20 |
| Acido palmitoleico | C16:1 | 0,3−3,5 |
| Acido eptadecanoico | C17:0 | ≤0,3 |
| Acido eptadecenoico | C17:1 | ≤0,3 |
| Acido stearico | C18:0 | 0,5−5,0 |
| Acido oleico | C18:1 | 55,0−83,0 |
| Acido linoleico | C18:2 | 2,5−21,0 |
| Acido α-linolenico | C18:3 | ≤1,0 |
| Acido arachidico | C20:0 | ≤0,6 |
| Acido gadoleico | C20:1 | ≤0,4 |
| Acido beenico | C22:0 | ≤0,2 |
| Acido lignocerico | C24:0 | ≤0,2 |
Acidi grassi insaturi e saturi
L’acido oleico è l’acido grasso più abbondante dell’olio d’oliva, con una concentrazione che, in base alle norme dell’International Olive Oil Council (IOOC) deve essere compresa tra il 55% e 83% del totale degli acidi grassi.[7]
L’acido linoleico è l’acido grasso polinsaturo più abbondante dell’olio di oliva, con una concentrazione che deve essere compresa tra il 2,5% e il 21% (IOOC). Dato il suo elevato grado di insaturazione, è facilmente soggetto a ossidazione; questo significa che un olio che ne contenga quantità elevate irrancidisce facilmente, e, dunque, può essere conservato per un tempo minore rispetto a un olio che ne contenga meno.[8]
Nella cucina mediterranea, l’olio di oliva è la principale fonte di grassi: dunque l’acido oleico, tra gli acidi grassi monoinsaturi, e il linoleico, tra i polinsaturi, sono i principali acidi grassi presenti.
L’acido α-linolenico deve essere presente in quantità molto bassa, secondo gli standard IOOC (≤1%). È uno degli acidi grassi polinsaturi omega-3, e può apportare benefici dal punto di vista nutrizionale. Tuttavia, a causa della forte insaturazione, al pari dell’acido linoleico, è suscettibile a ossidazione, e quindi favorisce l’irrancidimento dell’olio che lo contiene.
Gli acidi grassi saturi costituiscono circa il 15−25% del totale degli acidi grassi.
I più abbondanti sono l’acido palmitico (P, 7,5−20%) e l’acido stearico (S, 0,5−5%); in tracce possono essere presenti anche l’acido miristico, l’acido eptadecanoico, l’acido arachidico, l’acido beenico e l’acido lignocerico.
La presenza di acidi grassi che non dovrebbero essere presenti, o che dovrebbero essere presenti in percentuali diverse rispetto a quelle osservate, sono indici di adulterazione dell’olio, che è stato “tagliato” con altri oli di semi. A questo riguardo, particolare attenzione viene rivolta agli acidi miristico, arachidico, beenico, lignocerico, gadoleico e α-linolenico, le cui percentuali ammissibili sono specificate dal regolamento IOOC.[6]
Fattori che influenzano il profilo degli acidi grassi
La composizione in acidi grassi è influenzata da diversi fattori:
- il clima;
- la latitudine;
- la zona di produzione.
Gli oli prodotti in Italia, Spagna e Grecia sono ricchi in acido oleico e poveri in acido linoleico e palmitico, mentre l’olio tunisino è ricco in acido linoleico e palmitico e più povero di acido oleico. Dunque, gli oli d’oliva possono essere suddivisi in due gruppi:
Altri fattori che influenzano sono:
Va notato che l’acido oleico è formato per primo nel frutto, e i dati sembrano indicare un forte rapporto antagonistico tra l’acido oleico e gli acidi palmitico, palmitoleico e linoleico.[8]
Trigliceridi
Come detto in precedenza, gli acidi grassi dell’olio di oliva sono quasi per intero legati a formare molecole di trigliceridi.
In piccola percentuale si ritrovano anche presenti come digliceridi, monogliceridi, e in forma libera.[12]
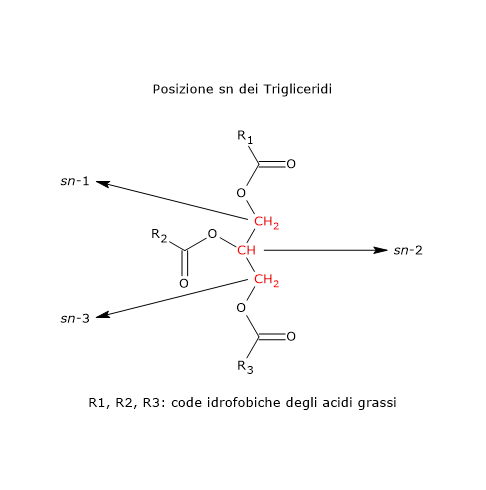
Durante la biosintesi dei trigliceridi, grazie alla presenza di specifici enzimi, solo circa il 2% delle molecole del glicerolo legherà in posizione sn-2 una molecola di acido palmitico. Anche la percentuale di acido stearico in posizione sn-2 è molto bassa. Per la maggior parte la posizione sn-2 è occupata dall’acido oleico.[4][13]
Al contrario, se si considerano oli che abbiano subito processi di esterificazione non enzimatica (artificiale), mancando la specificità dell’azione enzimatica, la percentuale di acido palmitico in posizione sn-2 aumenta in modo significativo.[11]
Nota: sn- è l’acronimo dell’inglese sterospecific numbering, che significa numerazione sterospecifica.
L’abbondanza relativa dei trigliceridi dell’olio d’oliva è ben caratterizzata e standardizzata dall’Olive Oil Council. Tra i trigliceridi presenti in proporzioni significative, i seguenti sono i più abbondanti:
- OOO (40−59%);
- POO (12−20%);
- OOL (12,5−20%);
- POL (5,5−7%);
- SOO (3−7%).
Si ritrovano anche quantità minori di POP, POS, OLnL, OLnO, PLL, PLnO.[6]
La trilinoleina (LLL) è un trigliceride contenente tre molecole di acido linoleico. Un suo basso livello è indice di buona qualità dell’olio.
Non sono stati osservati trigliceridi con soli acidi grassi saturi e neppure contenenti solo residui di acido α-linolenico.[14]
Digliceridi e monogliceridi
La loro presenza è dovuta sia a una incompleta sintesi dei trigliceridi che a parziali reazioni di idrolisi dei trigliceridi.
La concentrazione dei digliceridi nell’olio di oliva vergine varia tra l’1% e il 2,8%. Nell’olio fresco prevalgono gli 1,2-digliceridi, rappresentando oltre l’80% del totale dei digliceridi.[15]
Nel corso della conservazione dell’olio si verifica una isomerizzazione con un progressivo incremento della forma 1,3, più stabile, che dopo circa 10 mesi diviene la forma principale. Dunque, il rapporto 1,2/1,3-digliceridi può essere utilizzato come indicatore del grado di invecchiamento dell’olio.
I monogliceridi sono presenti in quantità inferiori rispetto ai digliceridi, meno dello 0,25%, con gli 1-monogliceridi ben più abbondanti dei 2-monogliceridi.[16]
Frazione insaponificabile
Questa frazione è composta da un elevato numero di molecole differenti con un ruolo nutrizionale chiave, in quanto contribuiscono in modo considerevole a quelli che sono gli effetti salutari dell’olio di oliva. Inoltre, sono responsabili della stabilità e del sapore dell’olio di oliva e sono utilizzati anche per determinarne una eventuale adulterazione con altri oli.[4]
Vi si ritrovano tocoferoli, steroli, polifenoli, pigmenti, idrocarburi, alcoli aromatici e alifatici, acidi triterpenici, cere e composti minori.[17]
Il loro contenuto è influenzato da fattori in parte analoghi a quelli che influenzano la composizione in acidi grassi, quali:
- il cultivar;
- il grado di maturazione delle olive;
- la zona di produzione;
- l’anno e le modalità di raccolta delle olive;
- il tempo di conservazione delle olive;
- il processo di estrazione dell’olio;
- le condizioni di conservazione dell’olio.[11]
Da sottolineare che negli oli di oliva raffinati molti di questi composti non sono presenti in quanto rimossi durante il processo di raffinazione.[11]
Polifenoli
I polifenoli rappresentano il 18−37% della frazione insaponificabile.
Sono un gruppo molto eterogeneo di molecole con proprietà nutrizionali e organolettiche; ad esempio, l’oleuropeina e l’idrossitirosolo danno all’olio un gusto amaro e pungente.[5][18]
Per una più ampia trattazione si rimanda all’articolo: Polifenoli dell’olio di oliva.
Idrocarburi
Rappresentano il 30−50% della frazione insaponificabile.
I principali sono lo squalene e il β-carotene.[19]
Lo squalene, isolato per la prima volta dal fegato di squalo, è il principale componente della frazione insaponificabile, e rappresenta oltre il 90% della frazione idrocarburica. La sua concentrazione oscilla tra i 200 e i 7500 mg/kg di olio d’oliva.[20]
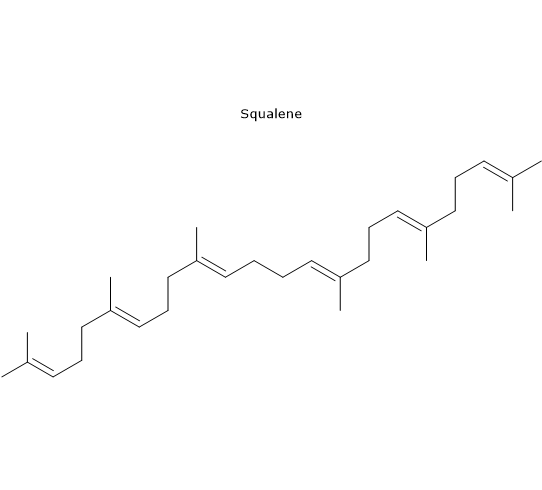
È un intermedio nella via di sintesi del nucleo a 4 anelli degli steroidi e sembra essere responsabile di molti dei benefici per la salute attribuiti all’olio di oliva.[21]
Nella frazione idrocarburica dell’olio vergine di oliva, oltre allo squalene, si ritrovano anche idrocarburi diterpenici e triterpenici, poliolefine isoprenoidi e n-paraffine.[22]
Steroli
Sono un importante gruppo di lipidi dell’olio di oliva che hanno:
- diversi effetti salutari;
- si correlano con la qualità dell’olio;
- sono ampiamente utilizzati per testarne la genuinità.
A questo riguardo c’è da sottolineare il fatto che gli steroli sono molecole specie specifiche, per cui trovare, ad esempio, nell’olio di oliva elevate concentrazioni di brassicasterolo, uno sterolo tipico delle Brassicaceae, come la colza, indica una sua adulterazione con olio di canola.[11]
Nell’olio di oliva sono presenti quattro classi di steroli: steroli comuni, 4-metilsteroli, alcoli triterpenici, e dialcoli triterpenici.[22] Il loro contenuto totale nell’olio d’oliva oscilla tra 1000 mg/kg, il valore minimo richiesto dagli standard IOOC, e 2000 mg/kg. I valori più bassi si osservano negli oli raffinati, dove il processo di raffinazione può causare perdite anche del 25%.[6][23][24]
Steroli comuni o 4-α-desmetilsteroli
Gli steroli comuni sono presenti per la maggior parte in forma libera ed esterificata, sebbene siano stati rinvenuti anche come lipoproteine e sterilglucosidi.
I principali sono il β-sitosterolo, che rappresenta il 75–90% del totale degli steroli, il Δ5-avenasterolo, 5–20%, e il campesterolo, circa il 4%.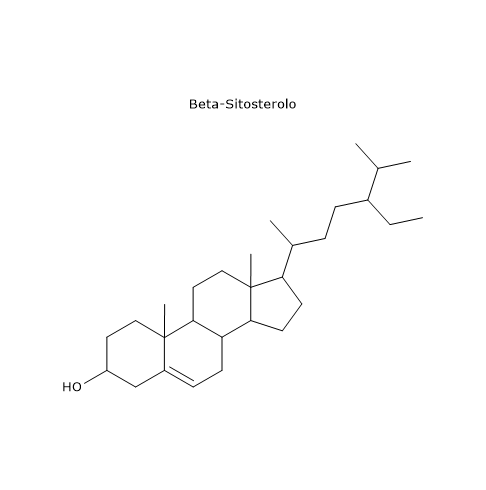 Altre molecole presenti in quantità inferiori o in tracce sono lo stigmasterolo, circa il 2%, colesterolo, brassicasterolo ed ergosterolo.[24]
Altre molecole presenti in quantità inferiori o in tracce sono lo stigmasterolo, circa il 2%, colesterolo, brassicasterolo ed ergosterolo.[24]
4-Metilsteroli
Sono intermedi nella biosintesi degli steroli e si ritrovano sia in forma libera che esterificata.[24]
Sono presenti in piccole quantità, molto minori rispetto a quelle degli steroli comuni e degli alcol triterpenici, oscillando tra 50 e 360 mg/kg. Le molecole principali sono l’obtusifoliolo, il gramisterolo, cicloeucalenolo e il citrostadienolo.[22]
Alcoli triterpenici o 4,4-dimetilsteroli
Sono una classe molto complessa di steroli, presenti sia in forma libera che esterificata.
Sono presenti in quantità variabili tra 350 e 1500 mg/kg.
I principali sono la β-amirina, il butirrospermolo, il 24-metilencicloartanolo e il cicloartenolo.
Altre molecole, presenti in quantità inferiori o in tracce, includono il ciclobranolo, il ciclosadolo, il dammaradienolo e il germanicolo.[22]
Dialcoli triterpenici
I principali dialcoli triterpenici dell’olio di oliva sono l’eritrodiolo e l’uvaolo.
L’eritrodiolo si trova sia in forma libera che esterificata; nell’olio vergine di oliva il suo contenuto è compreso tra i 19 e i 69 mg/kg, mentre la forma libera è in genere inferiore a 50 mg/kg.[22][23]
Tocoferoli
I tocoferoli rappresentano il 2−3% della frazione insaponificabile e includono la vitamina E.[4]
Degli otto vitameri della vitamina E, nell’olio di oliva vergine l’α-tocoferolo costituisce circa il 90% dei tocoferoli. È’ presente in forma libera e in quantità molto variabile, ma comunque in media superiore ai 100 mg/kg d’olio.[25] Grazie alle sue proprietà antiossidanti in vivo, la sua presenza è un fattore protettivo per la salute.[26]
La concentrazione dell’α-tocoferolo sembra essere correlata agli alti livelli di clorofille e alla concomitante richiesta di disattivazione dell’ossigeno singoletto.[27]
β-tocoferolo, δ-tocoferolo e γ-tocoferolo sono in genere presenti in piccole quantità.[22]
Pigmenti
In questo gruppo si ritrovano le clorofille e i carotenoidi.
Nell’olio di oliva, le clorofille sono presenti come feofitine, in particolare come feofitina A, ossia una molecola di clorofilla in cui il magnesio è stato rimosso e sostituito da due ioni idrogeno, e conferiscono all’olio d’oliva il caratteristico colore verde.
Agiscono come fotosensibilizzatori, per cui contribuiscono alla foto-ossidazione dell’olio stesso.[28][29]
I principali carotenoidi sono il β-carotene e la luteina. Sono presenti anche xantofille, quali anteraxantina, β-criptoxantina, luteoxantina, mutatoxantina, neoxantina e violaxantina.[30]
Il colore dell’olio di oliva è dovuto alla presenza di clorofille e carotenoidi e alle loro tonalità combinate di verde e giallo.[31]
Acidi triterpenici
Sono componenti importanti dell’oliva e sono presenti in tracce nell’olio.
I principali acidi triterpenici presenti nell’olio vergine di oliva sono l’acido oleanolico e l’acido maslinico. Si trovandono nella sansa e sono estratti in piccola quantità durante la lavorazione.[32]
Alcoli alifatici e aromatici
I più importanti sono gli alcoli grassi e gli alcoli diterpenici.
Gli alcoli alifatici hanno un numero di atomi di carbonio pari, compreso tra 20 e 30, e per la maggior parte sono localizzati all’interno del nocciolo, da dove sono parzialmente estratti attraverso processi meccanici.[4]
Alcoli grassi
Sono alcoli saturi lineari con più di 16 atomi di carbonio.
Possono essere presenti sia in forma libera che esterificata. Sono presenti nell’olio vergine di oliva in quantità di solito non superiori a 250 mg/kg.
I principali sono il docosanolo, il tetracosanolo, l’esacosanolo, e l’octacosanolo. Tetracosanolo ed esacosanolo sono quelli presenti in quantità maggiore.
Le cere, componenti minori dell’olio di oliva, sono esteri degli alcol grassi con acidi grassi. Le principali cere presenti sono esteri dell’acido palmitico e oleico. Possono essere utilizzate come criterio per differenziare i vari tipi di olio di oliva; ad esempio, in accordo con gli standard stabiliti dalla IOOC, nell’olio vergine ed extravergine di oliva devono essere presenti in quantità inferiori a 150 mg/kg.[11]
Alcoli diterpenici
Fitolo e geranilgeraniolo sono due alcol diterpenici aciclici, presenti sia in forma libera che esterificata.
Tra gli esteri nella frazione cerosa dell’olio extravergine di oliva si ritrovano quelli con l’oleato, eicosanoato, eicosenoato, docosanoato e tetracosanoato, principalmente in forma di fitil derivati.[11]
Composti volatili
Nell’olio di oliva sono stati identificati oltre 280 composti volatili, tra cui idrocarburi, i più abbondanti, alcoli, aldeidi, chetoni, esteri, acidi, eteri e altri. Tuttavia, solo circa 70 sono presenti a livelli superiori alla soglia di percezione, oltre la quale le molecole contribuiscono all’aroma dell’olio vergine di oliva.[33][34]
Componenti minori
Tra i componenti minori dell’olio di oliva si trovano fosfolipidi, di cui i principali sono la fosfatidilcolina, la fosfatidiletanolamina, il fosfatidilinositolo e la fosfatidilserina.
Possono essere presenti, negli oli non filtrati, quantità minime di proteine.[4]
Bibliografia
- ^ National Center for Biotechnology Information. PubChem Compound Summary for Olive Oil. https://pubchem.ncbi.nlm.nih.gov/compound/Olive-Oil. Accessed Nov. 13, 2025.
- ^ Codex Alimentarius Commission. Codex standard for olive oils and olive pomace oils (CXS 33-1981). Rome: FAO/WHO; 2019. Available from: https://www.fao.org/fao-who-codexalimentarius/
- ^ Mazzocchi A., Leone L., Agostoni C., Pali-Schöll I. The secrets of the Mediterranean diet. Does [only] olive oil matter? Nutrients 2019;11(12):2941. doi:10.3390/nu11122941
- ^ a b c d e f g Gunstone F.D. Vegetable oils in food technology: composition, properties and uses. 2nd Edition. Wiley J. & Sons, Inc., Publication, 2011.
- ^ a b Bulotta S., Celano M., Lepore S.M., Montalcini T., Pujia A., Russo D. Beneficial effects of the olive oil phenolic components oleuropein and hydroxytyrosol: focus on protection against cardiovascular and metabolic diseases. J Transl Med 2014;12:219. doi:10.1186/s12967-014-0219-9
- ^ a b c d International Olive Council. Trade standard applying to olive oils and olive-pomace oils (COI/T.15/NC No 3/Rev. 16, 2021). Madrid: International Olive Council; June 2021. Available from: https://www.internationaloliveoil.org/wp-content/uploads/2021/07/COI-T15-NC3-REV-16-2021-_ENG.pdf
- ^ a b Tomé-Rodríguez S., Barba-Palomeque F., Ledesma-Escobar C.A., Miho H., Díez C.M., Priego-Capote F. Influence of genetic and interannual factors on the fatty acids profile of virgin olive oil. Food Chem 2023;422:136175. doi:10.1016/j.foodchem.2023.136175
- ^ a b Hernández M.L., Sicardo M.D., Belaj A., Martínez-Rivas J.M. The oleic/linoleic acid ratio in olive (Olea europaea L.) fruit mesocarp is mainly controlled by OeFAD2-2 and OeFAD2-5 genes together with the different specificity of extraplastidial acyltransferase enzymes. Front Plant Sci 2021;12:653997. doi:10.3389/fpls.2021.653997
- ^ Cetinkaya H., Kulak M. Soil characteristics influence the fatty acid profile of olive oils. Scientific Papers. Series B, Horticulture. 2016;60:53-57. Available at: https://www.researchgate.net/publication/387363822
- ^ Ben Hmida R., Gargouri B., Chtourou F., Sevim D., Bouaziz M. Fatty acid and triacyglycerid as markers of virgin olive oil from mediterranean region: traceability and chemometric authentication. Eur Food Res Technol 2022;248:1-16. doi:10.1007/s00217-022-04002-1
- ^ a b c d e f g Boskou D. Olive oil: chemistry and technology. 3rd Edition, AOCS Press, 2015.
- ^ Lukić I., Da Ros A., Guella G., Camin F., Masuero D., Mulinacci N., Vrhovsek U., Mattivi F. Lipid profiling and stable isotopic data analysis for differentiation of extra virgin olive oils based on their origin. Molecules 2019;25(1):4. doi:10.3390/molecules25010004
- ^ Karupaiah T., Sundram K. Effects of stereospecific positioning of fatty acids in triacylglycerol structures in native and randomized fats: a review of their nutritional implications. Nutr Metab (Lond) 2007;4:16. doi:10.1186/1743-7075-4-16
- ^ Jawad M.A., Jawhar A., Dakah A., Ejbara M.G. Effect of maturity stages on triglyceride and fatty acid profiles in olive oil from Zaity and Kaissy varieties grown in Syria. Sci Rep 2025;15(1):35935. doi:10.1038/s41598-025-20162-y
- ^ International Olive Council. Determination of composition of triacylglycerols and content of di-acylglycerols by capillary gas chromatography. COI/T.20/Doc. No 32. Madrid: International Olive Council; November 2013. Available from https://www.internationaloliveoil.org/wp-content/uploads/2022/10/COI-T20-Doc.32-2013-Eng.pdf
- ^ Caponio F., Bilancia M.T., Pasqualone A., Sikorska E., Gomes T. Influence of the exposure to light on extra virgin olive oil quality during storage. Eur Food Res Technol 2005;221:92-98. doi:10.1007/s00217-004-1126-8
- ^ Talarico I.R., Bartella L., Rocio-Bautista P., Di Donna L., Molina-Diaz A., Garcia-Reyes J.F. Paper spray mass spectrometry profiling of olive oil unsaponifiable fraction for commercial categories classification. Talanta 2024;267:125152. doi:10.1016/j.talanta.2023.125152
- ^ Servili M., Sordini B., Esposto S., Urbani S., Veneziani G., Di Maio I., Selvaggini R. and Taticchi A. Biological activities of phenolic compounds of extra virgin olive oil. Antioxidants 2014;3:1-23. doi:10.3390/antiox3010001
- ^ Barp L., Miklavčič Višnjevec A., Moret S. Analytical determination of Squalene in extra virgin olive oil and olive processing by-products, and its valorization as an ingredient in functional food – A critical review. Molecules 2024;29(21):5201. doi:10.3390/molecules29215201
- ^ Hernández M.L., Muñoz-Ocaña C., Posada P., et al. Functional characterization of four olive squalene synthases with respect to the squalene content of the virgin olive oil. J Agric Food Chem 2023;71(42):15701-15712. doi:10.1021/acs.jafc.3c05322
- ^ Ibrahim N., Fairus S., Zulfarina M.S., Naina Mohamed I. The efficacy of squalene in cardiovascular disease risk – A systematic review. Nutrients 2020;12(2):414. doi:10.3390/nu12020414
- ^ a b c d e f Jimenez-Lopez C., Carpena M., Lourenço-Lopes C., Gallardo-Gomez M., Lorenzo J.M., Barba F.J., Prieto M.A., Simal-Gandara J. Bioactive compounds and quality of extra virgin olive oil. Foods 2020;9(8):1014. doi:10.3390/foods9081014
- ^ a b International Olive Council. Determination of the composition and content of sterols and triterpene dialcohols by capillary gas chromatography. COI/T.20/Doc. No 30/Rev. 2 – 2017. Madrid: International Olive Council; 2017. Available from: https://www.internationaloliveoil.org/wp-content/uploads/2022/10/COI-T20-Doc.30-rev.-2-2017-Eng.pdf
- ^ a b c Lukić M., Lukić I., Krapac M., Sladonja B., Piližota V. Sterols and triterpene diols in olive oil as indicators of variety and degree of ripening. Food Chem 2013;136(1):251-8. doi:10.1016/j.foodchem.2012.08.005
- ^ Beltrán G., Jiménez A., del Rio C., Sánchez S., Martínez L. Variability of vitamin E in virgin olive oil by agronomical and genetic factors. J Food Compos Anal 2010;23(6):633-639. doi:10.1016/j.jfca.2010.03.003
- ^ Sánchez-Villegas A., Sánchez-Tainta A. Virgin olive oil. In the prevention of cardiovascular disease through the
Mediterranean diet. Academic Press. Cambridge, MA, USA, 2018;59-87. - ^ Grams G.W., Eskins K. Dye-sensitized photooxidation of tocopherols. Correlation between singlet oxygen reactivity and vitamin E activity. Biochemistry 1972;11(4):606-8. doi:10.1021/bi00754a020
- ^ Giuliani A., Cerretani L., Cichelli A. Chlorophylls in olive and in olive oil: chemistry and occurrences. Crit Rev Food Sci Nutr 2011;51(7):678-90. doi:10.1080/10408391003768199
- ^ Díez-Betriu A., Bustamante J., Romero A., Ninot A., Tres A., Vichi S., Guardiola F. Effect of the storage conditions and freezing speed on the color and chlorophyll profile of premium extra virgin olive oils. Foods 2023;12(1):222. doi:10.3390/foods12010222
- ^ Gandul-Rojas B., Roca M., Gallardo-Guerrero L. Chlorophylls and carotenoids in food products from olive tree. In: Boskou D., Clodoveo M.L. Products from Olive Tree. IntechOpen, London, 2016. doi:10.5772/64688
- ^ Borello E., Roncucci D., Domenici V. Study of the evolution of pigments from freshly pressed to ‘on-the-shelf’ extra-virgin olive oils by means of near-UV visible spectroscopy. Foods 2021;10(8):1891. doi:10.3390/foods10081891
- ^ Sánchez-Quesada C., López-Biedma A., Warleta F., Campos M., Beltrán G., Gaforio J.J. Bioactive properties of the main triterpenes found in olives, virgin olive oil, and leaves of Olea europaea. J Agric Food Chem 2013;61(50):12173-82. doi:10.1021/jf403154e
- ^ Nardella M., Moscetti R., Bedini G., Bandiera A., Chakravartula S.S.N., Massantini R. Impact of traditional and innovative malaxation techniques and technologies on nutritional and sensory quality of virgin olive oil – A review. Food Chem Adv
Volume 2023;2:100163. doi:10.1016/j.focha.2022.100163 - ^ Angerosa F., Servili M., Selvaggini R., Taticchi A., Esposto S., Montedoro G. Volatile compounds in virgin olive oil: occurrence and their relationship with the quality. J Chromatogr A 2004;1054(1-2):17-31. doi:10.1016/j.chroma.2004.07.093