Gli isoflavoni sono polifenoli privi di colore appartenenti alla famiglia dei flavonoidi.
A differenza della maggior parte degli altri flavonoidi, hanno una distribuzione tassonomica limitata, trovandosi quasi esclusivamente nelle piante appartenenti alla famiglia delle Leguminose o Fabacee, in particolare nella soia.
Poiché i legumi, la soia in primis, sono una parte importante della dieta in molte culture, questi flavonoidi potrebbero avere un grande impatto sulla salute umana.
Si trovano anche nei fagioli e nelle fave, ma in concentrazioni molto minori rispetto a quelle presenti nella soia e nei prodotti derivati.
Un’altra buona fonte di tali molecole è il trifoglio rosso o trifoglio dei prati (Trifolium pratense), anch’esso appartenente alla famiglia delle Leguminose.
Nella frutta e verdura, al momento, non ne sono stati trovati.
Insieme agli acidi fenolici, quali l’acido caffeico e l’acido gallico, e ai glicosidi della quercetina, sono i polifenoli meglio assorbiti, seguiti dalle catechine (ma non le gallocatechine) e dai flavanoni.
Nelle piante alcuni isoflavoni sono dotati di attività antimicrobica e sono sintetizzati in risposta ad attacchi da parte di batteri o funghi; agiscono quindi come fitoalesine.
Indice
Struttura chimica
Mentre nella maggior parte dei flavonoidi l’anello B si lega all’anello C in posizione 2, negli isoflavoni l’anello B si lega all’anello C in posizione 3.
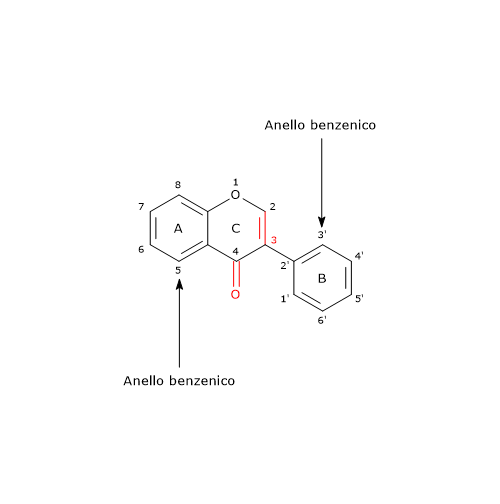
Anche se non sono steroidi, sono strutturalmente simili agli estrogeni, in particolare all’estradiolo. Questo conferisce loro proprietà pseudormonali, compresa la capacità di legarsi ai recettori per gli estrogeni, e sono per questo considerati fitoestrogeni o estrogeni vegetali. I benefici spesso ascritti alla soia e ai cibi a base di soia, ad esempio il tofu, si ritiene derivino dalla capacità degli isoflavoni presenti di agire come fitoestrogeni.
Va però sottolineato che il legame ai recettori per gli estrogeni sembra perdere forza con il tempo, per cui la loro efficacia non andrebbe sopravvalutata.
Negli alimenti sono presenti in quattro forme:
- aglicone;
- 7-O-glucoside;
- 6’-O-acetil-7-O-glucoside;
- 6’-O-malonil-7-O-glucoside.
Isoflavoni della soia: genisteina, daidzeina e gliciteina
La soia e i suoi derivati, come il latte, il tofu, il tempeh e il miso, sono la principale fonte di isoflavoni nella dieta umana.
Il contenuto in isoflavoni della soia e dei prodotti derivati varia in modo considerevole in funzione della zona geografica e delle condizioni di crescita e lavorazione; ad es. la soia ne contiene tra 580 e 3800 mg/kg di peso fresco mentre il latte di soia tra i 30 e i 175 mg/L.
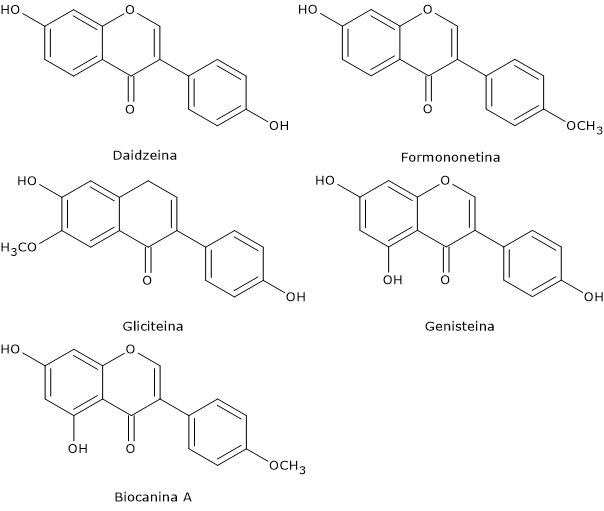
I più abbondanti in questi alimenti sono la genisteina, la daidzeina e la gliciteina, in genere presenti in rapporto di concentrazione 1:1:0,2; altri isoflavoni presenti sono la biocanina A e la formononetina.
I 6’-O-malonil derivati hanno un gusto sgradevole, amaro e astringente, e quindi conferiscono un cattivo sapore ai cibi in cui sono contenuti. Tuttavia, essendo sensibili alla temperatura, sono spesso idrolizzati a glicosidi nel corso dei processi industriali, come la produzione del latte di soia.
I processi di fermentazione che sono necessari nella preparazione di cibi come il tempeh e il miso determinano a loro volta l’idrolisi dei glicosidi ad agliconi, ossia la molecola priva di zucchero.
I glicosidi degli isoflavoni della soia e dei prodotti della soia possono essere deglicosilati anche per azione delle β-glicosidasi dell’intestino tenue umano.
Gli agliconi sono molto resistenti al calore.
Sebbene molti composti presenti nella dieta siano convertiti dai batteri intestinali in molecole meno attive, in altri casi si verifica la conversione in molecole dotate di maggiore attività biologica. Questo è il caso degli isoflavoni, ma anche dei prenilflavonoidi del luppolo (Humulus lupulus), e dei lignani, anch’essi fitoestrogeni.
Fitoestrogeni e menopausa
Nelle donne in perimenopausa, anche detta transizione menopausale, e in menopausa vera e propria, i sintomi vasomotori, come le vampate di calore e le sudorazioni notturne, e la perdita di massa ossea sono molto comuni. La terapia sostitutiva ormonale (TOS) si è dimostrata un trattamento molto efficace per queste problematiche.
Il ricorso a terapie alternative a base di fitoestrogeni è aumentato a seguito della pubblicazione dei risultati del “Women’s Health Initiative” (WHI), i quali suggeriscono che la terapia sostitutiva ormonale potrebbero portare più rischi, in particolare un aumento della probabilità di sviluppare di alcune malattie croniche, che benefici.
Tra i fitoestrogeni più utilizzati dalle donne in menopausa ci sono gli isoflavoni della soia, spesso assunti in forma di alimenti fortificati o compresse. Molti studi hanno però messo in evidenza la mancanza di efficacia degli isoflavoni di soia, e del trifoglio rosso, anche in grandi dosi, nella prevenzione dei sintomi vasomotori, quali le vampate di calore e sudorazioni notturne, e della perdita di massa ossea durante la menopausa.
Bibliografia
- de la Rosa L.A., Alvarez-Parrilla E., Gonzàlez-Aguilar G.A. Fruit and vegetable phytochemicals: chemistry, nutritional value, and stability. 1th Edition. Wiley J. & Sons, Inc., Publication, 2010
- Han X., Shen T. and Lou H. Dietary polyphenols and their biological significance. Int J Mol Sci 2007;9:950-988. doi:10.3390/i8090950
- Lagari V.S., Levis S. Phytoestrogens for menopausal bone loss and climacteric symptoms. J Steroid Biochem Mol Biol 2014;139:294-301 doi:10.1016/j.jsbmb.2012.12.002
- Lethaby A., Marjoribanks J., Kronenberg F., Roberts H., Eden J., Brown J. Phytoestrogens for menopausal vasomotor symptom. Cochrane Database of Systematic Reviews 2013, Issue 12. Art. No.: CD001395. doi:10.1002/14651858.CD001395.pub4
- Levis S., Strickman-Stein N., Ganjei-Azar P., Xu P., Doerge D.R., Krischer J. Soy isoflavones in the prevention of menopausal bone loss and menopausal symptoms: a randomized, double-blind trial. Arch Intern Med 2011:8;171(15):1363-1369 doi:10.1001/archinternmed.2011.330
- Manach C., Scalbert A., Morand C., Rémésy C., and Jime´nez L. Polyphenols: food sources and bioavailability. Am J Clin Nutr 2004;79(5):727-747. doi:10.1093/ajcn/79.5.727
- Tsao R. Chemistry and biochemistry of dietary polyphenols. Nutrients 2010;2:1231-1246. doi:10.3390/nu2121231