Le proantocianidine o tannini condensati, chiamate anche picnogenoli o leucocianidine, sono una sottogruppo di polifenoli, e in particolare di flavonoidi, ampiamente distribuito nel regno vegetale, e seconde solo alla lignina come fenolo più abbondante in natura.
Sono presenti in elevata concentrazione in varie parti delle piante come i fiori, i frutti, le bacche, i semi, come i semi d’uva, e la corteccia, ad esempio quella del pino.
Insieme agli antociani e i loro prodotti di ossidazione, e alle catechine, sono i flavonoidi più abbondanti nella dieta dell’uomo ed è stato suggerito che costituiscano una frazione significativa dei polifenoli ingeriti nella dieta occidentale.
Dunque i tannini condensati vanno presi in considerazione quando si studia l’associazione epidemiologica tra l’assunzione di polifenoli, in particolare dei flavonoidi, e le malattie croniche.
Indice
Struttura chimica
Le proantocianidine hanno una struttura chimica complessa essendo oligomeri, da dimeri a pentameri, o polimeri, da sei o più unità fino a 60, delle catechine o flavanoli, legate tra di loro da ponti carbonio-carbonio.
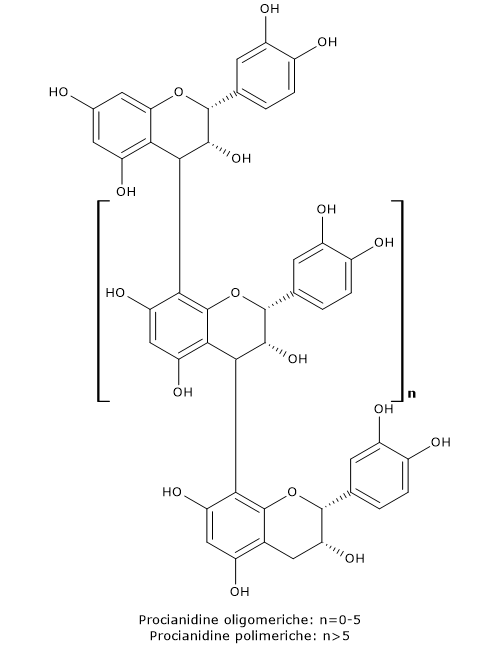
Possono essere costituite da sole subunità di:
- (epi)catechina, e sono definite procianidine;
- (epi)afzelechina, e sono definite propelargonidine;
- (epi)gallocatechina, e sono definite prodelfinidine.
Propelargonidine e prodelfinidine sono meno frequenti in natura e nei cibi rispetto alle procianidine.
In base ai legami che si stabiliscono tra i monomeri le proantocianidine posso avere una struttura definita:
- di tipo B se la polimerizzazione avviene tramite legame carbonio-carbonio tra la posizione 8 dell’unità terminale e la 4 della successiva o tra le posizioni 4 e 6;
- di tipo A, meno frequente, se i monomeri sono doppiamente legati tramite un legame etere C2-O-C7 o C2-O-C5 e un legame di tipo B.
Procianidine
I dimeri più comuni sono procianidine di tipo B, da B1 a B8, formati da catechina o epicatechina, unite da legami C4-C8, da B1 a B4, o C4-C6,da B5 a B8.
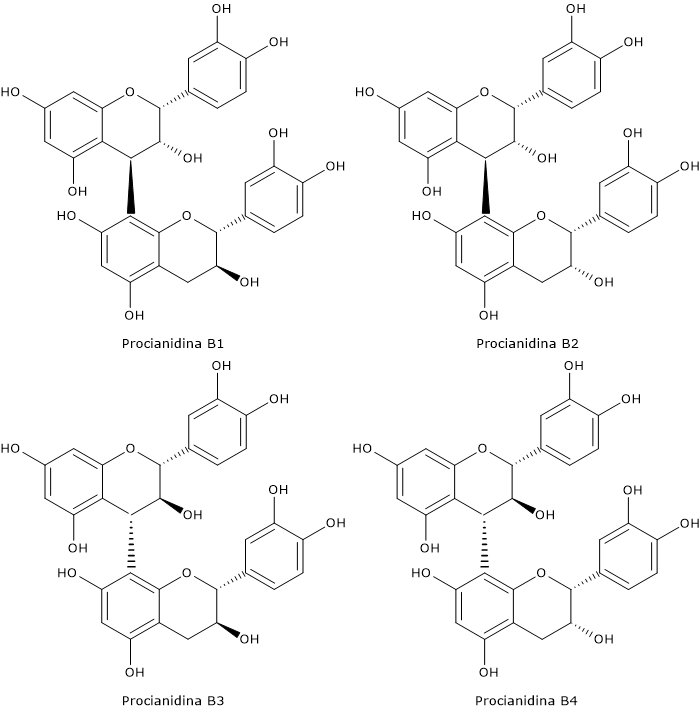
La procianidina C1 è un trimero di tipo B.
La procianidina A2 è un esempio di procianidina di tipo A.
Assorbimento intestinale
I tannini condensati sono scarsamente assorbiti a livello intestinale e, con gli antociani e i derivati esteri con l’acido gallico delle catechine del tè, sono i polifenoli meno ben assorbiti.
Sembra che gli oligomeri a basso peso molecolare, formati da 2-3 monomeri, possano essere assorbiti come tali mentre i polimeri non lo sono.
Nella circolazione sistemica i dimeri raggiungono concentrazioni di due ordini di grandezza inferiori rispetto a quelle delle catechine.
Le proantocianidine con un grado di polimerizzazione maggiore di tre sembra attraversino lo stomaco e l’intestino tenue senza significative modificazioni, per poi essere catabolizzate dal microbiota intestinale, che è parte del più ampio microbiota umano. I prodotti di degradazione includono gli acidi fenilacetico, fenilpropionico e fenilvalerico, acidi fenolici che sono stati suggeriti essere i principali metaboliti delle proantocianidine oligomeriche e polimeriche negli esseri umani sani.
Procianidine e catechine
In passato era stato proposto che il catabolismo intestinale delle procianidine portasse alla liberazione di catechine monomeriche, contribuendo così al loro pool sistemico negli esseri umani.
In realtà è stato dimostrato che ciò non accade in quanto le procianidine non contribuiscono in maniera significativa:
- alla concentrazione dei metaboliti delle catechine nella circolazione sistemica;
- al totale dei metaboliti delle catechine escreti con le urine;
- infine, non influenzano in modo significativo il profilo dei metaboliti plasmatici derivanti dall’attività della catecol-O-metiltransferasi.
Pertanto quando si vanno ad analizzare i potenziali effetti benefici sulla salute associati all’assunzione di cibi contenenti questi fitochimici, catechine e procianidine debbono essere considerate classi distinte di composti correlati.
Bibliografia
- de la Rosa L.A., Alvarez-Parrilla E., Gonzàlez-Aguilar G.A. Fruit and vegetable phytochemicals: chemistry, nutritional value, and stability. 1th Edition. Wiley J. & Sons, Inc., Publication, 2010
- Gu L., Kelm M.A., Hammerstone J.F., Beecher G., Holden J., Haytowitz D., Gebhardt S., and Prior R.L. Concentrations of proanthocyanidins in common foods and estimations of normal consumption. J Nutr 2004;134(3):613-617. doi:10.1093/jn/134.3.613
- Han X., Shen T. and Lou H. Dietary polyphenols and their biological significance. Int J Mol Sci 2007;9:950-988. doi:10.3390/i8090950
- Manach C., Scalbert A., Morand C., Rémésy C., and Jime´nez L. Polyphenols: food sources and bioavailability. Am J Clin Nutr 2004;79(5):727-747. doi:10.1093/ajcn/79.5.727
- Nandakumar V., Singh T., and Katiyar S.K. Multi-targeted prevention and therapy of cancer by proanthocyanidins. Cancer Lett 2008;269(2):378-387. doi:10.1016/j.canlet.2008.03.049
- Ottaviani J.I., Kwik-Uribe C., Keen C.L., and Schroeter H. Intake of dietary procyanidins does not contribute to the pool of circulating flavanols in humans. Am J Clin Nutr 2012;95:851-858. doi:10.3945/ajcn.111.028340
- Santos-Buelga C. and Scalbert A. Proanthocyanidins and tannin-like compounds: nature, occurrence, dietary intake and effects on nutrition and health. J Sci Food Agr 2000;80(7):1094-1117. doi:10.1002/(SICI)1097-0010(20000515)80:7<1094::AID-JSFA569>3.0.CO;2-1
- Tsao R. Chemistry and biochemistry of dietary polyphenols. Nutrients 2010;2:1231-1246. doi:10.3390/nu2121231
- Wang Y.,Chung S., Song W.O., and Chun O.K. Estimation of daily proanthocyanidin intake and major food sources in the U.S. diet. J Nutr 2011;141(3):447-452. doi:10.3945/jn.110.133900